 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
化学反应N2(g)+3H2(g)=2NH3(g),其定压反应热Qp和定容反应热Qv的相对大小
化学反应N2(g)+3H2(g)=2NH3(g),其定压反应热Qp和定容反应热Qv的相对大小是()。
A.Qp<Qv
B.Qp>Qv
C.Qp=Qv
D.无法确定
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
化学反应N2(g)+3H2(g)=2NH3(g),其定压反应热Qp和定容反应热Qv的相对大小是()。
A.Qp<Qv
B.Qp>Qv
C.Qp=Qv
D.无法确定
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“化学反应N2(g)+3H2(g)=2NH3(g),其定压反应…”相关的问题
更多“化学反应N2(g)+3H2(g)=2NH3(g),其定压反应…”相关的问题
A.1:1:1
B.1:0.5:0.33
C.2:1:0.66
D.不能确定
压强变化不会使下列化学反应的平衡移动的是()。
A.Hz(g) +I2(g) ==2HI(g)
B.3H2(g) +N2(g) ==2NH3(g)
C.2SO2(g) +O2(g) ==2S03(g)
D.C(S) +CO2(g) ==2CO(g)
O(1),写出有关反应式,利用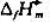 数据计算N2H4(1)的摩尔燃烧热.
数据计算N2H4(1)的摩尔燃烧热.
在77.2K时,用微球型硅酸铝催化剂吸附N2(g),在不同的平衡压力下,测得每千克催化剂吸附的N2(g)在标准状况下的体积数据如下:

已知77.2K时N2(g)的饱和蒸气压为99.125kPa,每个N2分子的截面积a=16.2x10-20m2.
试用BET公式计算该催化剂的比表面积.
可逆反应 达到化学平衡时:
达到化学平衡时:
(1)升高温度,反应标准平衡常数(),其原因是();
(2)在温度不变的条件下压缩气体的体积而增大压力时,I(g)的解离度().其原因是();
(3)恒容条件下充入N2,I2(g)的解离度(),其原因是()。
(4)恒压条件下充入N2,I2(g)的解离度(),其原因是()。
化学反应如下:
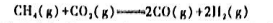
(1)利用教材附录中各物质的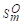 ,Δt
,Δt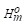 数据,求上述反应在25℃时的
数据,求上述反应在25℃时的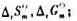
(2)利用教材附录中各物质的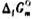 数据,计算上述及应在25℃时的
数据,计算上述及应在25℃时的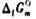 ;
;
(3)25℃,若始态CH4(g)和H2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的ΔtSm,ΔtGm.