 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K和标准状态时,下列反应均为非自发反应,其中在高温时仍为非自发的反应是( )。
A.Ag2O(s)=2Ag(s)+ O2(g)
O2(g)
B.N2O2=2NO2(g)
C.6C(s)+6H2O(g)=C6H12O6(s)
D.Fe2O3(s)+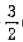 C(s)=2Fe(s)+
C(s)=2Fe(s)+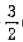 CO2g
CO2g
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Ag2O(s)=2Ag(s)+ O2(g)
O2(g)
B.N2O2=2NO2(g)
C.6C(s)+6H2O(g)=C6H12O6(s)
D.Fe2O3(s)+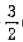 C(s)=2Fe(s)+
C(s)=2Fe(s)+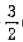 CO2g
CO2g
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在298K和标准状态时,下列反应均为非自发反应,其中在高温时…”相关的问题
更多“在298K和标准状态时,下列反应均为非自发反应,其中在高温时…”相关的问题
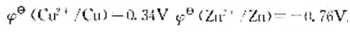 ,求此时原电池的电动势比标准状态时的电动势()
,求此时原电池的电动势比标准状态时的电动势()A.上升0.24V
B.下降0.24V
C.上升0.12V
D.下降0.12V
已知下列100kPa,298K时的热力学数据:
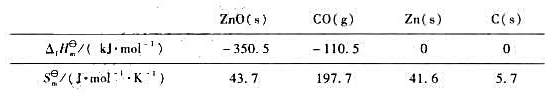
(1)试通过热力学计算,说明下面反应298K时的进行方向:
ZnO(s)+C(s)=Zn(s)+CO(g)
(2)求算上面反应自发正向进行的最低温度。
已知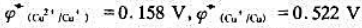 ,请计算反应2Cu+=Cu2++Cu在298K时的反应平衡常数.并由此说明+1价简单Cu+阳离子能否稳定存在于水溶液中?
,请计算反应2Cu+=Cu2++Cu在298K时的反应平衡常数.并由此说明+1价简单Cu+阳离子能否稳定存在于水溶液中?
298K时,在Fe3+,Fe2+的混合溶液中加入NaOH时,有Fe(OH)3和Fe(OH)2沉淀生成(假如没有其它反应发生)。当沉淀反应达到平衡时,保持c(OH-)=1.0molL-1,计算

应
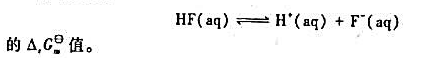
已知电对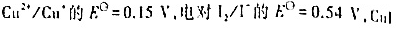 的
的
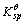 =1.3×10-12。
=1.3×10-12。
(1)试求氧化还原反应
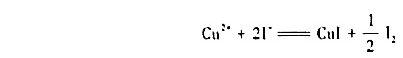
298K时的平衡常数;
(2)若溶液中Cu2+的起始浓度为0.10 mol·dm-3,I-的起始浓度为1.0 mol·dm-3,试计算达到平街时留在溶液中Cu2+的浓度。
水的质子自递反应,已知在18℃时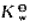 =6.4×10-15,25℃时
=6.4×10-15,25℃时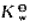 =1.0×10-14.
=1.0×10-14.
下列说法正确的是()。
A.水的质子自递反应是放热过程
B.水的质子自递反应是减反应
C.在18℃时,水的pH小于25℃时的pH
D.在18℃时,水中H+的浓度是8.0×10-8mol·L-1
2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g)
根据教材附录中的数据。计算反应在298K时的标准摩尔焓变 。若反应的热能完全转化为势能, 可将100kg的重物垂直升高多少?已知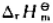 (N2H4,l)=50.63kJ·mol-1.
(N2H4,l)=50.63kJ·mol-1.
某基元反应:A→B其活化能Ea=60.4kg·mol-1,逆反应的活化能E'a=95.6kg·mol-1,
(1)试结合图1.18.1所示的反应进程-势能图,定性判断该反应是吸热反应,还是放热反应,求算该反应的ΔtH;
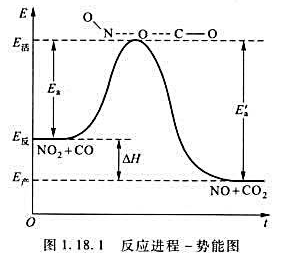
(2)若298K时的速率常数k=2.3×10-2s-1。试求373K时的速率常数;
(3)求算阿伦尼乌斯公式中的指前因子A。