 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算pH=10.0,总浓度为0.10mol·L-1NH3-NH4Cl缓冲溶液中Ag+/Ag电对的条件电势。=0.80V,的lgβ[1=3.24,lgβ2=7.05
计算pH=10.0,总浓度为0.10mol·L-1NH3-NH4Cl缓冲溶液中Ag+/Ag电对的条件电势。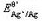 =0.80V,
=0.80V,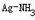 的lgβ[1=3.24,lgβ2=7.05,pKb(NH3)=4.74;忽略离子强度及形成
的lgβ[1=3.24,lgβ2=7.05,pKb(NH3)=4.74;忽略离子强度及形成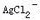 络合物的影响]
络合物的影响]
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算pH=10.0,总浓度为0.10mol·L-1NH3-NH4Cl缓冲溶液中Ag+/Ag电对的条件电势。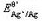 =0.80V,
=0.80V,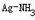 的lgβ[1=3.24,lgβ2=7.05,pKb(NH3)=4.74;忽略离子强度及形成
的lgβ[1=3.24,lgβ2=7.05,pKb(NH3)=4.74;忽略离子强度及形成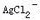 络合物的影响]
络合物的影响]
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算pH=10.0,总浓度为0.10mol·L-1NH3-N…”相关的问题
更多“计算pH=10.0,总浓度为0.10mol·L-1NH3-N…”相关的问题
计算pH=10.0,在总浓度为0.1mol·L-1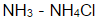 缓冲溶液中,Ag+/Ag电对的条件电势。忽略离子强度及形成
缓冲溶液中,Ag+/Ag电对的条件电势。忽略离子强度及形成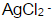 络合物的影响。(Ag-NH3络合物的lgβ1~lgβ2分别为3.24、7.05;
络合物的影响。(Ag-NH3络合物的lgβ1~lgβ2分别为3.24、7.05;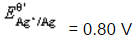 。)
。)
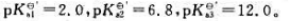
在pH=10.0的氨性缓冲溶液中,含有浓度均为2.0×10-2mol·L-1的Mg2+和Zn2+。今加入KCN掩蔽其中的Zn2+,再以2.0×10-2mol·L-1EDTA滴定此混合溶液25.0mL中的Mg2+。若检测终点时,△pMg=0.2,欲使终点误差Et=0.1%,问应加入KCN多少克?(lgKZnY=16.5,lgKMgY=8.7;pH=10.0时,lgαY(H)=0.45;HCN的pKa=9.21;Zn2+-CN-络合物的lgβ4=16.7,M(KCN)=65.1g·mol-1)
00mol/L),计算滴定至化学计量点时的pCu+和pCu值(已知lgKCuY=18.8,pH=10.0时,lgαCu(OH)=0.8,lgαY(H)=0.5,Cu-NH3配合物的各数累积常数lgβ1~lgβ4:4.13、7.61、10.48、12.59)
A.A、B两溶液的aZn(NH3)不相等
B.A、B两溶液的aZn(OH)相等
C.A、B两溶液的[Zn2+`]相等
D.A、B两溶液的[Zn2+]相等
计算pH=5时EDTA的酸效应系数及对数值。若此时EDTA各种型体总浓度为0.02mol/L,求[Y4-]。
A.温度一定时,影响缓冲溶液pH值的主要因素为pKa和缓冲比
B.缓冲溶液的有效缓冲范围为pKa±1
C.缓冲溶液缓冲比一定时,总浓度越大,则其缓冲容量越大
D.缓冲溶液加水稀释后,pH值基本不变,缓冲容量也不变
A.当总浓度一定时,缓冲比为1时β值最大
B.缓冲溶液稀释后缓冲比不变,所以pH不变,β也不变
C.缓冲溶液的有效缓冲范围为pKa±1
D.缓冲溶液的缓冲能力是在一定范围内的