 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
金属钾具有体心立方密堆积结构,如下面左图所示;金属铂具有立方最密堆积结构,如下面右图所示。
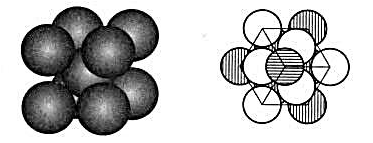
(1)试计算金属晶体中钾原子的空间占有率;
(2)试计算金属晶体中铂原子的空间占有率;
(3)已知铂的相对原子质量为195.08,若金属铂的立方晶胞的边长a=392.3pm,试计算每立方厘米金属铂的质量。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)

(1)试计算金属晶体中钾原子的空间占有率;
(2)试计算金属晶体中铂原子的空间占有率;
(3)已知铂的相对原子质量为195.08,若金属铂的立方晶胞的边长a=392.3pm,试计算每立方厘米金属铂的质量。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“金属钾具有体心立方密堆积结构,如下面左图所示;金属铂具有立方…”相关的问题
更多“金属钾具有体心立方密堆积结构,如下面左图所示;金属铂具有立方…”相关的问题
(1)画出C60的ccp结构沿四重轴方向的投影图;并用分数坐标示出分子间多面体空隙中心的位置(每类多面体空隙中心只写一组坐标即可)。
(2)在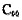 的ccp和hcp结构中,各种多面体空隙理论上所能容纳的“小球"的最大半径是多少?
的ccp和hcp结构中,各种多面体空隙理论上所能容纳的“小球"的最大半径是多少?
(3)C60分子还可形成非最密堆积结构,使某些碱金属离子填入多面体空隙,从而制得超导材料。在K3C60所形成的立方面心晶胞中,K+占据什么多面体空隙?占据空隙的百分数为多少?
已知氧化铁FexO(富氏体)为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。今有一批氧化铁,测得其密度为5.71gcm-3,用MoK射线(λ=71.07pm)测得其面心立方晶胞衍射指标为200的衍射角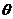 =9.56°(sin
=9.56°(sin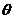 =0.1661,Fe的相对原子质量为55.85)。
=0.1661,Fe的相对原子质量为55.85)。
(1)计算FexO的面心立方晶胞参数;
(2)求x;
(3)计算Fe2+和Fe3+各占总铁量的质量分数;
(4)写出标明铁的价态的化学式。
已知NaCl的晶体结构如图C.17.1所示,它属于立方晶系,Oh点群。晶胞参数=564.0pm。
(I)写出通过晶胞中心的点对称元素。
(2)根据Na+和Cl-的离子半径值,了解在这结构中负离子是否接触?这种结构的稳定性如何?
(3)试计算NaCl晶体的密度D。
(4)将图C.17.1晶胞中顶角上的Na+和中心的Cl-除去,将Na+换成Nb2+,Cl-换得O2-即得NbO晶胞,试画出NbO的晶胞和其中原子簇的结构;已知晶跑参数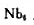 =421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
=421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
(5)将图C.17.1晶胞中面心和体心的原子除去,顶角上的Na+换成U6+,棱上的Cl-换成O2-,得UO3的晶体结构,立方晶胞参数a=415.6pm。试画出UO3晶胞的结构;写出通过晶胞中心点的点对称元素和点群;计算晶体的密度,计算U6+的离子半径(U的相对原子质量为238.0);画出由处在12条棱上的02-组成的立方八面体的图形;计算该多面体的自由孔径。