 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
NH3分子中,N原子的轨道杂化类型及NH3分子的空间构型是:()。
A.sp2杂化、正三角型
B.sp杂化、直线型
C.sp3杂化、V字型
D.sp3杂化、三角锥型
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.sp2杂化、正三角型
B.sp杂化、直线型
C.sp3杂化、V字型
D.sp3杂化、三角锥型
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“NH3分子中,N原子的轨道杂化类型及NH3分子的空间构型是:…”相关的问题
更多“NH3分子中,N原子的轨道杂化类型及NH3分子的空间构型是:…”相关的问题
A.电子在整个分子范围内运动,不再属于某一特定原子
B.反键分子轨道的能量比所有成键分子轨道高,此当反键分子轨道上有电子时,分子不稳定
C.分子轨道是不同原子的原子轨道线性组合面成,杂化轨道是同一原子的原子轨道组合而成
D.只有符合对称性匹配、能量相近和最大重叠原则的原子轨道才能有效地组合成分子轨道
试用价层电子对互斥理论判断出下列分子或离子的几何构型,并指出中心原子的轨道杂化方式:
(1)O3;(2)NO3-;(3)AsI5;(4)NH3;(5)IF5;(6)POCl3;
由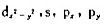 轨道组成dsp2等性杂化轨道
轨道组成dsp2等性杂化轨道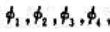 ,这些轨道极大值方向按平面四方形分别和x,y轴平行。根据原子轨道正交、归一性推出各个杂化轨道的d,s,px,py,的组合系数,验证它们是正交、归一的。
,这些轨道极大值方向按平面四方形分别和x,y轴平行。根据原子轨道正交、归一性推出各个杂化轨道的d,s,px,py,的组合系数,验证它们是正交、归一的。
试用VSEPR理论预测下列分子或离子的几何构型,并用杂化轨道理论加以说明:
①BeCl2;②SnCl2;③NCl3;④XeF4;⑤SF6;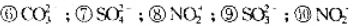
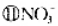 .
.