 更多“正反应是基元反应,那么逆反应也是基元反应。A正确B错误”相关的问题
更多“正反应是基元反应,那么逆反应也是基元反应。A正确B错误”相关的问题
第1题
某基元反应:A→B其活化能Ea=60.4kg·mol-1,逆反应的活化能E'a=95.6kg·mol卐
某基元反应:A→B其活化能Ea=60.4kg·mol-1,逆反应的活化能E'a=95.6kg·mol-1,
(1)试结合图1.18.1所示的反应进程-势能图,定性判断该反应是吸热反应,还是放热反应,求算该反应的ΔtH;
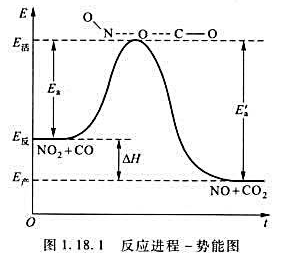
(2)若298K时的速率常数k=2.3×10-2s-1。试求373K时的速率常数;
(3)求算阿伦尼乌斯公式中的指前因子A。
第5题
使用质量作用定律的条件是()。A.基元反应B.非基元反应C.基元反应,非基元反应均可D.变温下发生的
使用质量作用定律的条件是()。
A.基元反应
B.非基元反应
C.基元反应,非基元反应均可
D.变温下发生的
第9题
对于非基元反应,()。A.速度方程可由化学方程式导出B.反应级数只能是正整数C.反应速度决定于最慢
对于非基元反应,()。
A.速度方程可由化学方程式导出
B.反应级数只能是正整数
C.反应速度决定于最慢的基元反应
D.一般由三个基元反应构成
第10题
在一定温度范围内,反应为基元反应。 (1)写出该基元反应的速率方程; (2)若其他条件不变,将容
在一定温度范围内,反应为基元反应。 (1)写出该基元反应的速率方程; (2)若其他条件不变,将容
点击查看答案
在一定温度范围内,反应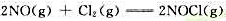 为基元反应。
为基元反应。
(1)写出该基元反应的速率方程;
(2)若其他条件不变,将容器的体积缩小到原来的1/2,反应速率如何变化?


 如果结果不匹配,请
如果结果不匹配,请 
















