题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知NH4CuSO3与足量的2 mol·L-1硫酸溶液混合微热,产生下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是()
A.反应中硫酸作氧化剂
B.NH4CuSO3中部分Cu元素被氧化
C.1 mol NH4CuSO3完全反应转移1 mol电子
D.刺激性气味的气体是氨气
 答案
答案
B、NH4CuSO3中部分Cu元素被氧化
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.反应中硫酸作氧化剂
B.NH4CuSO3中部分Cu元素被氧化
C.1 mol NH4CuSO3完全反应转移1 mol电子
D.刺激性气味的气体是氨气
 答案
答案
B、NH4CuSO3中部分Cu元素被氧化
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知NH4CuSO3与足量的2 mol·L-1硫酸溶液混合微…”相关的问题
更多“已知NH4CuSO3与足量的2 mol·L-1硫酸溶液混合微…”相关的问题
A.NaClO溶液的消毒原理是使蛋白质变性
B.1 mol Cl2与足量NaOH溶液反应转移2 mol电子
C.NaClO溶液的漂白原理与SO2相同
D.消毒后的餐具,晾干后可直接使用
A.NaClO溶液的消毒原理是HClO具有强氧化性
B.1 mol Cl2与足量NaOH溶液反应转移2 mol电子
C.NaClO溶液的漂白原理与Na2O2、活性炭相同
D.84消毒液与洁厕灵(盐酸)共同使用,可达到既清洁又消毒的双重效果
A.制乙酸乙酯时,向乙醇中缓慢加入浓硫酸和乙酸
B.可将导管插入饱和碳酸钠溶液中收集反应生成的乙酸乙酯
C.1 mol乙醇与2 mol乙酸在浓硫酸催化作用下不能合成1 mol乙酸乙酯
D.除去乙酸乙酯中含有的乙酸,最好的处理方法是用足量饱和碳酸钠溶液洗涤后分液
A.铁的反应速率=0.5 mol•L-1•min-1
B.硫酸的反应速率=0.25 mol•L-1•min-1
C.硫酸亚铁的生成速率=0.5 mol•L-1•min-1
D.氢气的反应速率=0.5 mol•L-1•min-1
钛(Ti)被称为继铁、铝之后的第三金属,四川攀枝花和西昌地区的钒钛磁铁矿储量十分丰富。如以下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。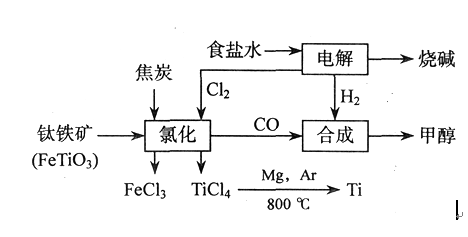 请填写以下空白:
请填写以下空白:
问题一、电解食盐水时,总反应的离子方程式是()。
问题二、写出钛铁矿经氯化法得到四氯化钛的化学方程式:()。
问题三、已知:①Mg(s)+Cl2(g)=MgCl2(s);△H=-641kJ/mol ②Ti(s)+2Cl2(g)=TiCl4(s);△H=-770kJ/mol。以下说法正确的选项是()。
AMg的燃烧热为641kJ/mol
BTi的能量一定比TiCl4高
C等质量的Mg(s)、Ti(s)与足量的氯气反应,前者放出的热量多
D该冶炼Ti法对环境友好
问题四、在上述产业链中,合成192t甲醇理论上需额外补充H2()t(不考虑生产过程中物质的任何损失)。
问题五、以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是()。
A.m=n/2
B.m=2n/3
C.m=3n/2
D.m=2n
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以制饮料
C.1 mol乙醇可生成1 mol乙醛
D.1 mol乙醇跟足量的Na作用得0. 5 mol H2
A.0.2 mol NO
B.0.2 mol NO2和0.05 mol N2O4
C.0.1 mol N2O
D.0.1 mol NO、0.1 mol NO2和0.1 mol N2O4
积25℃的甲醇与水进行混合.已知甲醇和水在25℃、30%(mol%)甲醇溶液的偏摩尔体积
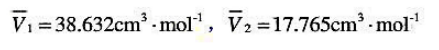
25℃下纯物质的体积