 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
回答下列问题 (1)在含有[Ag(NH3)2]+配离子的溶液中滴加盐酸时会发生什么现象?为什么? (2)[Co(SCN)4]2-的
回答下列问题
(1)在含有[Ag(NH3)2]+配离子的溶液中滴加盐酸时会发生什么现象?为什么?
(2)[Co(SCN)4]2-的稳定性比[Co(NH3)6]2+小,为什么在酸性溶液中[Co(SCN)4]2-可以存在,而[Co(NH3)6]2+却不能存在?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
回答下列问题
(1)在含有[Ag(NH3)2]+配离子的溶液中滴加盐酸时会发生什么现象?为什么?
(2)[Co(SCN)4]2-的稳定性比[Co(NH3)6]2+小,为什么在酸性溶液中[Co(SCN)4]2-可以存在,而[Co(NH3)6]2+却不能存在?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“回答下列问题 (1)在含有[Ag(NH3)2]+配离子的溶液…”相关的问题
更多“回答下列问题 (1)在含有[Ag(NH3)2]+配离子的溶液…”相关的问题
在0.1mol·L-1[Ag(NH3)2]+溶液中加入NaCl,使NaCl的浓度达到0.001mol·L-1时,问(1)有无AgCl沉淀出现?(2)在含有2mol·L-1氨水的0.1mol·L-1的[Ag(NH3)2]+溶液中加入NaCI,也使NaCl的浓度达到0.001mol·L-1时,问有无AgCl沉淀出现?(3)从两种情况中试得出必要的结论。
已知在化学式为Co(NH3)4Br(CO3)的配合物中,中心Co3+为六配位的八面体形结构,C022-作为配位体既可按单啮,也可按双啮进行配位。据此回答下列问题:
(1)根据配位体场的强弱,写出这个化合物的组成结构式;
(2)画出全部可能的异构体的立体结构;
(3)根据它们的什么性质可用实验方法来区分异构体。
硫化银精矿(含Ag2S,CuS,ZnS,PbS,Al2O3及SiO2等)氯化焙烧提银工艺如图所示: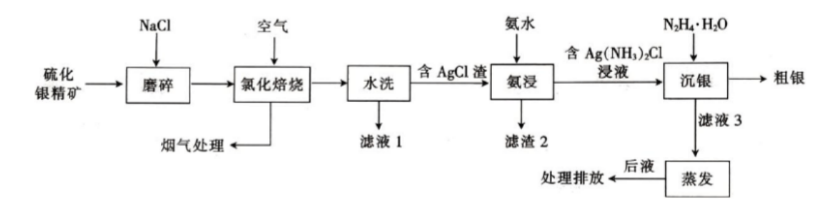 已知:氯化焙烧时,氧化物不参与反应,硫化物转化为氯化物;氯化铅不溶于水,溶于氯化钠溶液。
已知:氯化焙烧时,氧化物不参与反应,硫化物转化为氯化物;氯化铅不溶于水,溶于氯化钠溶液。
回答下列问题:
(1)硫化银精矿和食盐在氯化焙烧前需磨碎的目的是()。
(2)“氯化焙烧”时,金属硫化物在高温下先氧化为氧化物,再氯化为金属氯化物。
①Ag2S焙烧生成氧化银反应的化学方程式为()。
②“烟气处理”时,烟尘进行回收后,还需用碱液处理的目的是()。
(3)已知常温下,Ksp(AgCL)=1.8×10-10。“水洗”后,“滤液1”中c(Cl-)=0.05mol.L-1,则c(Ag+)=()mol.L-1。
(4)“滤渣2”主要为Al2O3和()(填化学式)。
(5)“滤液3”蒸发的目的是()。
(6)粗银(含Ag及少量Cu,Pb,Au等)可采用电解精炼提纯,用AgNO3,少量HNO3,KNO3配成电解液。电解时,阴极上有少量NO产生,其原因是()(用电极反应是解释)。
A.1.7×10-7
B.1.7×107
C.1.7×10-5
D.1.7×105
计算pH=10.0,总浓度为0.10mol·L-1NH3-NH4Cl缓冲溶液中Ag+/Ag电对的条件电势。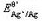 =0.80V,
=0.80V,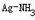 的lgβ[1=3.24,lgβ2=7.05,pKb(NH3)=4.74;忽略离子强度及形成
的lgβ[1=3.24,lgβ2=7.05,pKb(NH3)=4.74;忽略离子强度及形成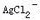 络合物的影响]
络合物的影响]
下列各个配位离子分别具有八面体(六配位)和四面体(四配位)构型,由它们组成的配合物哪些能给出顺磁共振信号。
(1)[Fe(H2O6)]2+;
(2)[Fe(CN)6]6-;
(3)[Fe(CN)6]3-;
(4)[CoF6]3-;
(5)[Co(en)3]3+;
(6)[C(N02)6]4-;
(7)[FeCl4]-;
(8)[Ag(NH3)4]+;
(9)[ZnCl4]2-。
比较AgCl在6mol·L-1氨水和水中的溶解度。已知KSP(AgCl)=1.8×10-10,KSP{[Ag(NH3)2]+}=1.12×107。
A.Al3+ K+ SO2-4 S2-
B.HCO- Cl- Na+ OH-
C.NO-3 ALO-2 OH- K+
D.[Ag(NH3)2]+ H+ Na+ S2-
某校化学研究性学习小组的同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原Cu0呢?他们设计实验制取氮气并探究上述问题。请你参与该小组的活动并完成下列研究:
(一)制取氨气
(1)写出实验制取氨气的化学方程式()。
(2有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的()(填“能”或“否”)。理由是()。
(二)该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性: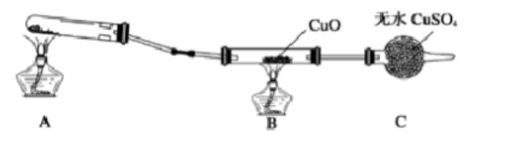 ⑴该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是:()。
⑴该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是:()。
(2)利用改进后的装置进行实验,观察到Cu0变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。写出氨气与Cu0反应的化学方程式()。
(三)问题讨论:
有同学认为:NH3与Cu0反应生成的红色物质中可能含有Cu20.已知:Cu20是一种碱性氧化物;在酸性溶液中,Cu'的稳定性差(Cu+→Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu0:()。