 更多“重量法则Mg2+时,应快速加入氨水, 以便迅速生成沉淀。”相关的问题
更多“重量法则Mg2+时,应快速加入氨水, 以便迅速生成沉淀。”相关的问题
A.Mg2+的含量
B.a2+的含量
C.e3+的含量
D.a2+和Mg2+的总量
A.增加流动相中甲醇的比例
B.增加流动相水中的比例
C.流动相中加入少量HAc
D.流动相中加入少量氨水
在pH=10.0的氨性缓冲溶液中,含有浓度均为2.0×10-2mol·L-1的Mg2+和Zn2+。今加入KCN掩蔽其中的Zn2+,再以2.0×10-2mol·L-1EDTA滴定此混合溶液25.0mL中的Mg2+。若检测终点时,△pMg=0.2,欲使终点误差Et=0.1%,问应加入KCN多少克?(lgKZnY=16.5,lgKMgY=8.7;pH=10.0时,lgαY(H)=0.45;HCN的pKa=9.21;Zn2+-CN-络合物的lgβ4=16.7,M(KCN)=65.1g·mol-1)
实验室以活性炭为催化剂,由CoCl2•6H2O制备(Co(NH3)6)Cl3的流程如图已知Co2+在pH=9.4时完全沉淀为Co(OH)2下列说法错误的是()。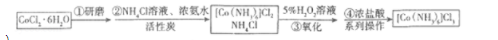
A.步骤①中“研磨”的目的是为了增大晶体的表面积,加快溶解速率
B.步骤②中应先加入浓氨水,再加入NH4Cl溶液
C.步骤③中发生的反应为2[Co(NH3)6]Cl2+2NH4Cl+H2O2═2[Co(NH3)6]Cl3+2NH3•H2O
D.步骤④中加入浓盐酸,有利于析出[Co(NH3)6]Cl3
A.Ca2+含量
B.Mg2+含量
C.Ca2+、Mg2+含量
D.Ca2+、Mg2+、Fe3+、Al3+总量
A.Ca2+的含量
B.Mg2+的含量
C.a2+、Mg2+、Fe2+、Al3+的总量
D.Ca2+、Mg2+的总量
A.Mg2+含量
B.Ca2+含量
C.Ca2+和Mg2+总量
D.Fe3+和Al3+总量
E. Al3+、Fe3+、Ca2+、Mg2+总量
在Al3+、Zn2+、Mg2+共存的酸性溶液中欲测定Mg2+,试指出以下分析步骤中的错误之处(简述理由),并改正。
吸取一定量试液于锥形瓶中,加入10%KCN 1mL,以NaOH溶液调节溶液的pH约等于10,加入1:3三乙醇胺15mL,再加入0.2%二甲酚橙指示剂2~3滴,以EDTA标准溶液滴至溶液由红紫变亮黄色为终点。


 如果结果不匹配,请
如果结果不匹配,请 
















