 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用Cl-选择性电极作负极,SCE作正极组成电池,测定某溶液中氯化物的含量。取100mL此溶液在25℃时测得电池电动势
用Cl-选择性电极作负极,SCE作正极组成电池,测定某溶液中氯化物的含量。取100mL此溶液在25℃时测得电池电动势为28.8mV,加入1.00mL浓度为0.475mol·L-1的经酸化的NaCl标准溶液后,测得电池电动势为53.5mV。求该溶液中氯化物的浓度(mol·L-1)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用Cl-选择性电极作负极,SCE作正极组成电池,测定某溶液中氯化物的含量。取100mL此溶液在25℃时测得电池电动势为28.8mV,加入1.00mL浓度为0.475mol·L-1的经酸化的NaCl标准溶液后,测得电池电动势为53.5mV。求该溶液中氯化物的浓度(mol·L-1)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用Cl-选择性电极作负极,SCE作正极组成电池,测定某溶液中…”相关的问题
更多“用Cl-选择性电极作负极,SCE作正极组成电池,测定某溶液中…”相关的问题
A.将反应2Fe3++Fe===3Fe2+设计为原电池,则可用Zn为负极,Fe为正极,FeCl3为电解质
B.铜片和铝片用导线连接后插入浓硝酸中,铜作负极
C.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
D.铝片和镁片用导线连接后插入NaOH溶液中,Mg较活泼作负极
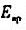 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。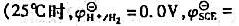
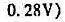
A.电池工作时,氧气发生氧化反应
B.电池正极的电极反应式:O2+2H2O+4e-=4OH-
C.电池负极的电极反应式:C8H18+25O2--50e-=8CO2↑+9H2O
D.若消耗的O2为11.2L(标准状况),则电池中有1 mol电子发生转移
A.控制溶液的pH在一定范围
B.使标液与试液的离子强度保持一致
C.掩蔽Fe3+、Al3+干扰离子
D.加快响应时间
A.干电池内发生的是氧化还原反应
B.锌为负极,碳为正极
C.工作时,电子由碳极经过外电路流向锌极
D.长时间连续使用时,内装糊状物可能流出腐蚀用电器
A.正极的电极反应为O2+2H2O+2e﹣=4OH﹣
B.负极的电极反应为Al+3OH﹣﹣﹣3e﹣═AI(OH)3↓
C.电池工作过程中,电解液的pH保持不变
D.电池使用时可能析出H2并放热
A.通CO的一极是电池的正极
B.负极发生的电极反应是O2+2CO2+4e-=2CO32-
C.负极发生的电极反应是CO+CO32--2e-=2CO2
D.正极发生氧化反应
A.锂电极作电池负极,放电过程中发生还原反应
B.1 mol SOCl2发生电极反应转移的电子物质的量为4 mol
C.组装该电池必须在无水、无氧的条件下进行
D.电池的正极反应为2SOCl2+2e-=4Cl-+S+SO2 ↑
A.根据反应Cu+H2SO4=CuSO4+H2↑设计的原电池中铜作负极
B.钠块与铜用导线连接后插入到稀盐酸中发现铜的表面很快有大量的气泡冒出
C.根据原电池原理,可以将反应2H2+O2=2H2O设计成原电池,且H2在负极反应
D.构成闭合回路是形成原电池的必备要素之一,电子在此闭合回路中从负极流经导线到达正极,再从正极经电解质溶液流回负极
用Ce4+标准滴定溶液滴定Fe2+应选择()作指示电极。
A.pH玻璃电极
B.银电极
C.氟离子选择性电极
D.铂电极