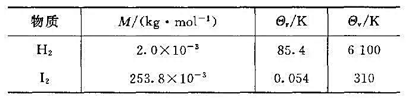题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知氮(N2,g)的摩尔定压热容与温度的函数关系为Cp,m=[27.32-6.226×10-3(T/K)+0.9502×10-6(T/K)2]J·mol-1·K-
已知氮(N2,g)的摩尔定压热容与温度的函数关系为Cp,m=[27.32-6.226×10-3(T/K)+0.9502×10-6(T/K)2]J·mol-1·K-1将始态为300K,100kPa下1mol的N2(g)置于1000K的热源中,求下列过程达到平衡态时的Q,△S及△Siso(1)恒压过程;(2)恒容过程。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“已知氮(N2,g)的摩尔定压热容与温度的函数关系为Cp,m=…”相关的问题
更多“已知氮(N2,g)的摩尔定压热容与温度的函数关系为Cp,m=…”相关的问题

 分别为52.3J·mol-1·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1。试由附录(在教材中)中各化合物的标准摩尔生成焓计算1000K时下列反应的
分别为52.3J·mol-1·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1。试由附录(在教材中)中各化合物的标准摩尔生成焓计算1000K时下列反应的 。
。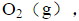
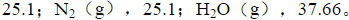 假设气体适用于理想气体状态方程。
假设气体适用于理想气体状态方程。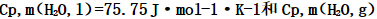
 求在25℃时水的摩尔蒸发焓。
求在25℃时水的摩尔蒸发焓。 ,摩尔定容热容
,摩尔定容热容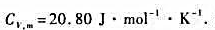 )
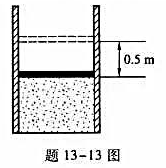
)
 =6.012kJ·mol-1.已知在-10~0℃范围内过冷水(H2O,l)和冰的摩尔定压热容分别为76.28J·mol-1·K-1和37.20J·mol-1·
=6.012kJ·mol-1.已知在-10~0℃范围内过冷水(H2O,l)和冰的摩尔定压热容分别为76.28J·mol-1·K-1和37.20J·mol-1·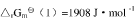

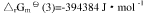
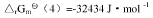 试求:(1)尿素CO(NH2)2(s)的标准摩尔生成Gibbs自由能
试求:(1)尿素CO(NH2)2(s)的标准摩尔生成Gibbs自由能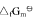 ;(2)由稳定单质生成尿素反应的平衡常数与上列反应平衡常数的关系式;(3)由单质生成尿素反应的平衡常数
;(2)由稳定单质生成尿素反应的平衡常数与上列反应平衡常数的关系式;(3)由单质生成尿素反应的平衡常数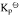 。
。