 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
向KOH溶液中通入11.2 L(标准状况)氯气恰好完全反应生成三种含氯盐: 0.7molKCl、0.2molKClO和X。则X是()
A.0.1molKClO4
B.0.1molKClO3
C.0.2molKClO2
D.0.1molKClO2
 答案
答案
B、0.1molKClO3
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.0.1molKClO4
B.0.1molKClO3
C.0.2molKClO2
D.0.1molKClO2
 答案
答案
B、0.1molKClO3
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“向KOH溶液中通入11.2 L(标准状况)氯气恰好完全反应生…”相关的问题
更多“向KOH溶液中通入11.2 L(标准状况)氯气恰好完全反应生…”相关的问题
A.0.75mol/L
B.1.5mol/L
C.2mol/L
D.3mol/L
能源是人类共同关注的重要问题。页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g)=CO(g)+3H2(g)△H1
已知:①CH4、H2、CO的燃烧热(△H)分别为-a()kJ•mol-1、-bkJ•mol-1、-ckJ•mol-1;②H2O(l)=H2O(g);△H=+dkJ•mol-1
则△H1=()(用含字母a、b、c、d的代数式表示)kJ•mol-1。
(2)用合成气生成甲醇的反应为:CO(g)+2H2(g)⇌CH3OH(g)△H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示:
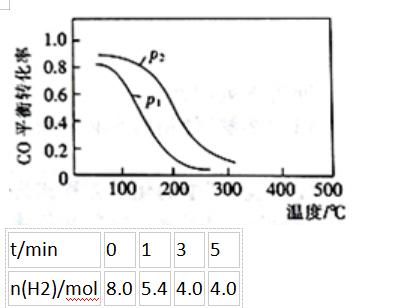 ①△H2()(填“>”“<”或“=”)0。
①△H2()(填“>”“<”或“=”)0。
②下列说法正确的是()(填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
③0〜3min内用CH3OH表示的反应速率v(CH3OH)=()mol•L-1·min-1。(计算结果保留两位有效数字)
④200℃时,该反应的平衡常数K=()。向上述200℃达到平衡的恒容密闭容器中再加入2molCO、2molH2、2molCH3OH,保持温度不变,则化学平衡()(填“正向”、“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6L甲烷,测得电路中转移1.2mol电子,则甲烷的利用率为()。
A.=3.36 时,CO2+2OH-=CO32-+H2O
B.=4.48 时,2CO2+3OH-=CO32-+HCO3-+H2O
C.=5.60 时,3CO2+4OH-=CO32-+2HCO3-+H2O
D.=6.72 时,CO2+OH-=HCO3-
A.KOH(aq)+1/2H2SO4(aq)===1/2K2SO4(aq)+H2O(l) ΔH=-11.46 kJ•mol-1
B.2KOH(aq)+H2SO4(aq)===K2SO4(aq)+2H2O(l) ΔH=-11.46 kJ·mol-1
C.2KOH(aq)+H2SO4(aq)===K2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
D.KOH(aq)+1/2H2SO4(aq)===1/2K2SO4(aq)+H2O(l) ΔH=-57.3 kJ•mol-1
A.(HCO3-)略大于c(CO32—)
B.能使酸性高锰酸钾溶液褪色
C.(Na+)等于c(CO32—)与c(HCO3—)之和
D.(HCO3—)略小于c(CO32—)
A.150mL
B.120mL
C.90mL
D.60mL
A.通入CH3OH的电极为负极
B.随着放电的进行,负极附近pH上升
C.每消耗1mol CH3OH可以向外电路提供6mol e﹣
D.通入O2的一极电极反应为4H2O+2O2﹣+8e﹣═8OH﹣
A.9.0L
B.13.5L
C.15.7L
D.16.8L